Étape 2
Amedeo Avogadro
Lorenzo Romano Amedeo Carlo Avogadro (Amedeo Avogadro) est un physicien et chimiste italien, né à Turin le 9 août 1776 et mort le 9 juillet 1856.

Découverte
Amedeo Avogadro a énoncé son hypothèse en 1811. Cette découverte a démontré la différence entre les atomes et les molécules. Celle-ci a marqué une période importante dans l'évolution de la chimie. S'appuyant sur la théorie atomique, la loi de Gay-Lussac et la loi de Dalton sur les rapports volumiques, son hypothèse est la suivante :
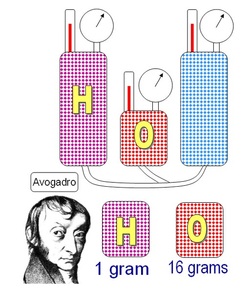
«Des volumes égaux de gaz différents, aux mêmes conditions de température et de pression, contiennent le même nombre de molécules».
De la sorte, il devient possible de déterminer la masse molaire d'un gaz à partir de celle d'un autre.La plus grande et importante difficulté qu'il doit surmonter concerne la confusion faite entre atomes et molécules à cette époque. L'une de ses contributions les plus importantes est de faire clairement la distinction entre les deux en admettant que les molécules peuvent être constituées d'atomes (distinction que ne fait pas John Dalton, par exemple). En réalité, Avogadro n'utilise pas le mot atome dans ses travaux (à l'époque, les termes atome et molécule sont utilisés de manière confuse), mais il considère qu'il existe trois sortes de molécules, dont l'une est une molécule élémentaire (atome). Il effectue aussi une distinction entre les termes de masse et de poids.
En 1814, Avogadro publie un Mémoire sur les masses relatives des molécules des corps simples, ou densités présumées de leur gaz, et sur la constitution de quelques-uns de leur composés, pour servir de suite à l'Essai sur le même sujet, publié dans le Journal de Physique, juillet 1811 qui s'intéresse à la densité des gaz.
En 1820, l'université de Turin crée pour lui une chaire de physique qu'il occupera jusqu'à son décès. En 1821, il publie un autre mémoire intitulé Nouvelles considérations sur la théorie des proportions déterminées dans les combinaisons, et sur la détermination des masses des molécules des corps et peu après Mémoire sur la manière de ramener les composés organiques aux lois ordinaires des proportions déterminées.
Le nom d'Avogadro reste attaché à celui du nombre d'Avogadro indiquant le nombre de molécules contenues dans une seule mole.
L’hypothèse qu’Avogadro a énoncé a été le résultat d'un développement extrêmement brillant :
1) les gaz sont compressibles et dilatables et il existe certainement de grands espaces entre leurs molécules;
2) les gaz ont les mêmes lois de compressibilité (loi de Mariotte) et de dilatation (loi de Gay-Lussac), il en résulte qu'ils doivent avoir le même nombre de "vides". Dans un volume donné, si le nombre de vides est équivalent, alors le nombre de molécules l’est aussi.
La loi d'Avogadro
Avogadro n'a pas vraiment pu donner une valeur aux nombres de molécules d'un atome, le nombre d'Avogadro a longtemps été une estimation expérimentale. De nos jours, la valeur la plus exacte est 6,023X10 exposant 23. Cette valeur a été découverte par Robert Millikan, un physicien américain, à l'aide du "pulvérisateur".
Le nombre d'Avogadro signifie le nombre de molécules présentes dans une molécule-gramme d'un composé et le nombre d'atomes contenus dans un atome-gramme d'un corps simple. À une température de 0 degrés Celsius et à une pression de 101,3 kPa, le nombre de molécules contenues dans 20 cm3 d'un gaz est constant. Ce nombre est égal à 6,023x10 exposant 23 molécules "nombre d'Avogadro" et son symbole est NA.
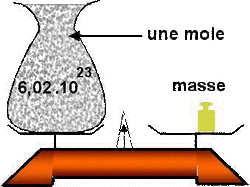
Exemple:
Récipient
| 1
| 2
| 3
|
À l'époque, l'hypothèse était mal reçue par les chimistes, parce qu’elle manquait de fondement expérimental et la différence entre les atomes et les molécules n'était pas très claire. En 1814, Ampère repris l'hypothèse, mais elle ne fut pas toujours reconnue. Ce n'est qu'environ en 1860, deux ans après la mort d'Avogadro, que Stanislas Cannizzaro, un élève d'Avogadro, arrive à faire triompher l'hypothèse de son maître au congrès international de chimie qui eut lieu à Karlsruhe, en Allemagne.
Impact sur la société
Grâce à cette découverte, nous savons maintenant qu'un atome et une molécule ne sont pas égaux. L'hypothèse nous a aussi montré que des gaz différents en même quantité, dans les mêmes conditions de température et de pression, contiennent la même quantité de molécules.
Aujourd'hui encore, nous utilisons le nombre d'Avogadro pour calculer le nombre de molécules dans les composés. Son hypothèse est enseignée et elle est aussi un sujet de recherche dans les écoles.
VIDÉO
Bibliographie
1) http://fr.wikipedia.org/wiki/Amedeo_Avogadro
2)http://mendeleiev.cyberscol.qc.ca/chimisterie/9703/VSauve.html
3)http://sites.estvideo.net/college.anne.fr/dossier2/pages2/pages_
copains_d_albert/page13_amedeo_avogadro_damien.htm

